 El ion consiste en un átomo o conglomerado de átomos que dependiendo el acontecimiento de haber obtenido o perdido electrones se añadieron una carga eléctrica, esto significa que los iones constituyen átomos que son imprecisos en el ámbito eléctrico.
El ion consiste en un átomo o conglomerado de átomos que dependiendo el acontecimiento de haber obtenido o perdido electrones se añadieron una carga eléctrica, esto significa que los iones constituyen átomos que son imprecisos en el ámbito eléctrico.
 Este acontecimiento de obtener o perder electrones en el área de química se denomina ionización, y es descrito como la división de los objetos unidos o moléculas en diferentes iones. Esencialmente, entonces, la ionización lo que hace, lo que crea, son iones y lo que anteriormente se explicaba de un átomo que consigue carga eléctrica, debido a que pierde o gana electrones.
Este acontecimiento de obtener o perder electrones en el área de química se denomina ionización, y es descrito como la división de los objetos unidos o moléculas en diferentes iones. Esencialmente, entonces, la ionización lo que hace, lo que crea, son iones y lo que anteriormente se explicaba de un átomo que consigue carga eléctrica, debido a que pierde o gana electrones.
Dentro de la ionización, es posible que se presenten dos clases: la ionización física y la ionización de tipo química.
Dentro de la biología de tipo molecular o en las compañías, los iones son fundamentales debido a que consisten en elementos importantes de los seres vivos o se emplean para generar máquinas precisas tales como motores.
Tipos de iones
Catión
 Los cationes se definen como iones con carga positiva, esto significa que son átomos con una carencia de electrones en los orbitales exteriores. Los componentes que generalmente tienen más capacidad de ionizarse de forma positiva, o sea, los elementos que usualmente pierden electrones engloban a los metales, sin embargo, esta propiedad puede verse en algunos no metales, entre otros elementos.
Los cationes se definen como iones con carga positiva, esto significa que son átomos con una carencia de electrones en los orbitales exteriores. Los componentes que generalmente tienen más capacidad de ionizarse de forma positiva, o sea, los elementos que usualmente pierden electrones engloban a los metales, sin embargo, esta propiedad puede verse en algunos no metales, entre otros elementos.
La extensión de los cationes es mínima, en comparación con los aniones y los átomos neutrales, esto se debe a su carencia de electrones en la capa exterior.
Anión
El anión consiste en una molécula que contiene carga eléctrica de tipo negativa, que se genera como producto de haber obtenido uno o más electrones. El anión es lo contrario al catión, que es un ión con una carga de tipo positiva.
Se han descubierto algunos beneficios de los aniones, estos incluyen: la incitación que genera en el conglomerado de células que tienen como labor proteger el cuerpo humano, esto se consigue ordenando y orientando la resistencia ante las enfermedades.
De igual forma, los aniones eliminan las bacterias: cuando no existe oxígeno, las bacterias se difunden, sin embargo, los aniones brindan el oxígeno apropiado para que las primeras bacterias no puedan continuar con vida.
Ion poliatómico
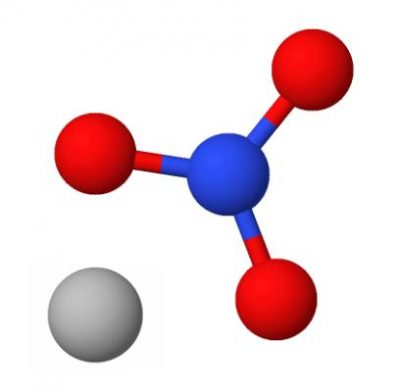 Los iones poliatómicos consisten en la agrupación de varios átomos que están unidos de forma química y poseen cargas negativas o positivas, y que son definidos como una unidad de los estímulos químicos.
Los iones poliatómicos consisten en la agrupación de varios átomos que están unidos de forma química y poseen cargas negativas o positivas, y que son definidos como una unidad de los estímulos químicos.
Esta clase de iones poliatómicos más usuales contienen cargas negativas. Esto quiere decir que el conglomerado de átomos ha conseguido electrones.
En la mayor cantidad de estos iones, hay un átomo central, en su derredor se encuentran el resto de los átomos. En muchas ocasiones son átomos de oxígenos los que envuelven el átomo central; cuando se produce esto, el ion es denominado oxoanión.
Ion monoatómico
El ion monoatómico es descrito como una molécula que posee una carga eléctrica. Este fenómeno ocurre debido a que la molécula ha perdido u obtenido electrones.
Zwitterión
Es un tipo de ion que posee de forma simultánea una zona con carga negativa y otra con carga positiva. Debido al componente salino que tiene, esta clase de ion es disoluble en agua. Cuando está en una mezcla acuosa, es posible categorizar un ion zwitterión como positivo, negativo o neutral.
Ion hidronio
Se considera un ion sencillo que procede de un estímulo químico entre una molécula de agua y un elemento ácido. El ion hidronio se puede ver en diversas formas, pudiendo ser líquido, gaseoso y sólido. Los iones hidronios existen en la atmosfera, sin embargo, es posible localizarlos en el espacio.
Usos de los iones
Los cationes y los aniones se consideran fundamentales para los seres vivientes y son otorgados por las sales minerales solubles en agua, éstas se vinculan los procedimientos químicos y los iones son empleados por el cuerpo para hacer labores que determinen su equilibrio.
La carencia de iones genera una desestabilización funcional, y genera enfermedades que si no se tratan pueden causar la muerte.